FDA公告:含阿利吉仑的降压药更改安全标签
来源: 发布时间:2012-04-28 13:43
4月20日,美国食品与药物管理局(FDA)发布公告称,在糖尿病或肾损害患者中,当使用含阿利吉仑的降压药与名为血管紧张素转化酶抑制剂(ACEI)和血管紧张素受体阻滞剂(ARB)的其他药物同时使用时,可能存在肾损伤、低血压及高钾血症的风险。
FDA添加了新的警告,以避免肾损害患者联合使用这些药物,阿利吉仑药物的标签正在更新。但在未咨询医师的情况下,正在接受含阿利吉仑药物治疗的患者不应擅自停用该类药物。
须修改安全性标签的药物有:
① Amturnide(阿利吉仑/氨氯地平/氢氯噻嗪),② Tekturna(阿利吉仑),③ Tekturna HCT(阿利吉仑/氢氯噻嗪),④ Tekamlo(阿利吉仑/氨氯地平),⑤ Valturna(阿利吉仑/缬沙坦)。
该警告是根据一项临床试验用心-肾终点的2型糖尿病阿利吉仑试验(ALTITUDE)的初步数据做出的。在ALTITUDE试验中,相对于一组服用安慰剂加一种ARB或ACEI的患者,服用阿利吉仑加一种ARB或ACEI的患者肾损害、低血压和高血钾水平(高钾血症)风险升高。数据还显示,阿利吉仑组的心血管事件(死亡或卒中)稍微过多(见数据概述),然而,FDA尚未就这些药物与死亡或卒中之间的真正关联做出明确的结论。FDA将会评估最终的试验结果和来自其他阿利吉仑试验的结果,并且将通告任何可用的新信息。
截至2012年4月20日,以下建议被添加至含阿利吉仑产品的药物标签:
• 糖尿病患者联用阿利吉仑、ARB或ACEI是一种新的禁忌症,因为存在肾损害、低血压和高钾血症的风险。
• 警告中至重度肾损害[即肾小球滤过率(GFR)< 60 mL/min]的患者避免同时使用阿利吉仑和ARB或ACEI。
数据概述
FDA评估了来自ALTITUDE(用心-肾终点的2型糖尿病阿利吉仑试验)6的初步数据,这是一项在批准阿利吉仑上市后进行的临床试验。由于缺乏疗效和观察到接受阿利吉仑治疗的糖尿病患者肾损害、低血压和高钾血症的风险大于接受安慰剂治疗的患者,因此ALTITUDE试验提前终止。以下信息描述了ALTITUDE中期试验结果。
ALTITUDE试验
用心-肾终点的2型糖尿病阿利吉仑试验(ALTITUDE)
ALTITUDE试验旨在确定(与安慰剂相比)阿利吉仑联合传统治疗是否能够减少心脏、循环系统和肾脏导致的死亡和疾病。伴有肾病的2型糖尿病患者(由存在白蛋白尿或GFR降低确定)被随机分组,接受阿利吉仑300 mg/d(n=4283)或安慰剂(n=4296)。所有患者均接受ARB或ACEI联合治疗。主要疗效转归是指主要复合终点(由心血管死亡、)的第1例事件出现的时间、猝死、非致死性心肌梗死、非致死性卒中、心力衰竭住院、终末期肾病、肾死亡以及血清肌酐浓度较基线水平翻倍,并且持续至少1个月。
对每例患者中位随访约27个月后,该试验因缺乏疗效而提前终止。如表1所示,与接受安慰剂治疗的患者相比,在阿利吉仑组观察到肾损害、低血压和高钾血症的风险较大。
表1 ALTITUDE参与患者不良反应的发生率
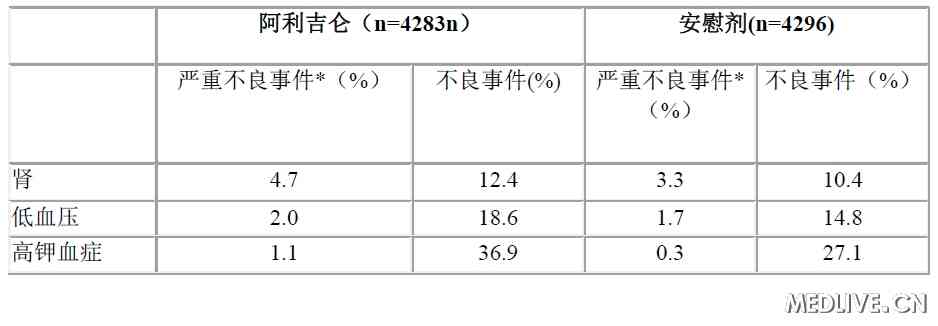
已获批的ACEI和ARB列表见表2和表3。
表2 已获批的血管紧张素转化酶抑制剂(ACEI)
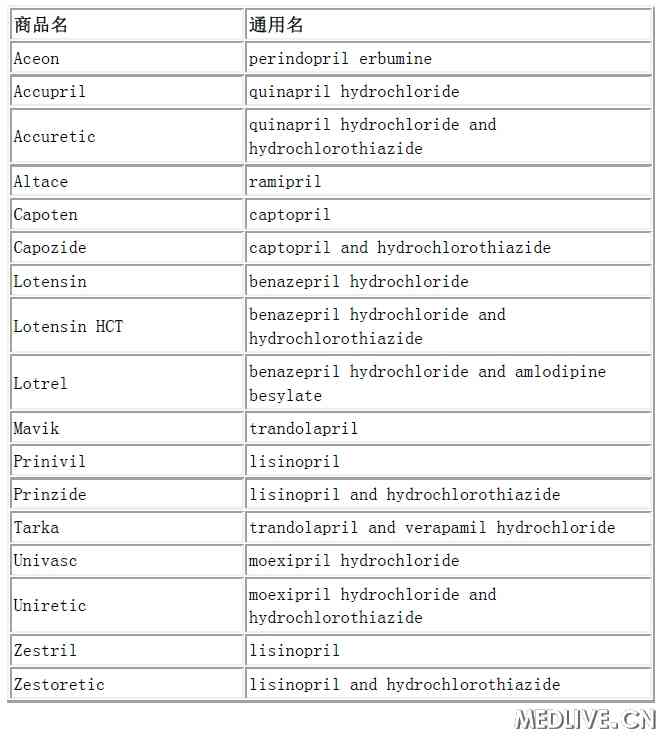
表3 已获批的血管紧张素受体阻滞剂(ARB)
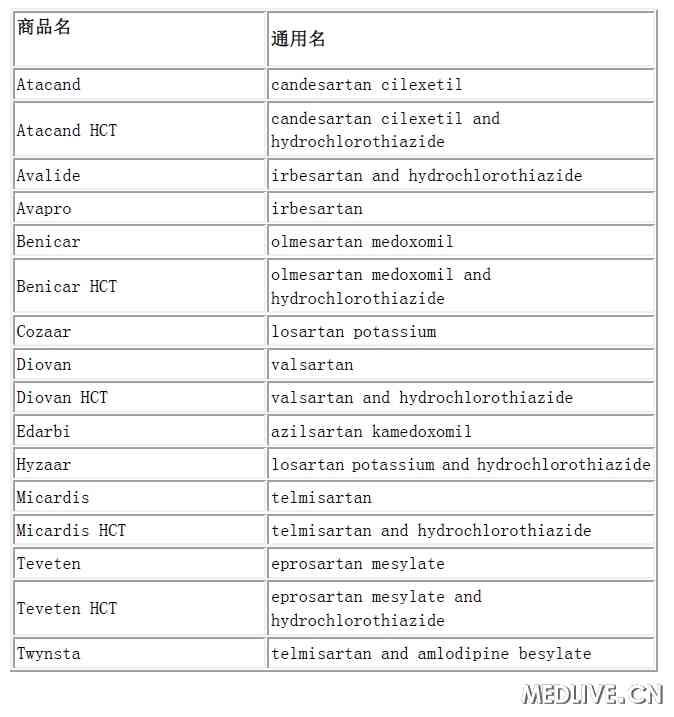

来源:医脉通

请先登录,先评论.