病例报告丨股静脉-房间隔途径经导管二尖瓣置换术一例
来源: 发布时间:2021-01-07 17:57

生物瓣膜衰败后二次开胸换瓣是导致心外科手术高风险的重要因素。2020 年美国心脏病学会/美国心脏协会(AHA)指南推荐经导管二尖瓣植入瓣中瓣作为高风险患者的替代方案。本文报道了 1 例 77 岁二尖瓣生物瓣衰败男性患者,经评估为外科高风险,行股静脉-房间隔途径的经导管二尖瓣置换。患者术后 3 h 在 CCU 拔除气管插管,无气促等不适,术后第 1 d 转出监护室,第 3 d 出院。相比心尖途径,股静脉-房间隔途径创伤更小,更早脱离监护室,更早康复出院。
临床资料
患者,男,77 岁,因“二尖瓣换瓣术后4 年,劳力性呼吸困难 2 年”就诊。入院 4 年前患者因“二尖瓣脱垂伴重度反流、卵圆孔未闭”在胸腔镜下行“二尖瓣生物瓣置换术及卵圆孔修补术”,植入瓣膜为 Biocor/Epic 25 猪生物瓣(St. Jude)。2 年前开始出现活动后呼吸困难,日常活动明显受限,6 个月前出现阵发性心房扑动,劳力性呼吸困难加重,复查彩色超声心动图提示:人工生物瓣衰败,跨瓣压差增大,外科评估再次手术风险大一直药物保守治疗。2 个月前呼吸困难加重收入我院。
既往有“2 型糖尿病、下肢静脉曲张、慢性萎缩性胃炎伴肠上皮化生、腹股沟斜疝修补术”等病史。
辅助检查:超声心动图提示左心室(LV)内径 38 mm,左心房(LA)内径 40 mm,右心室(RV)内径 30 mm,右心房(RA)内径 58 mm,射血分数(EF)58%,二尖瓣生物瓣增厚与运动减弱,跨瓣血流显著变窄、加速(Vmax=2.7 m/s),平均跨瓣压差高达13 mm Hg,有效瓣口面积 1.1 cm2,二尖瓣生物瓣膜毁损伴中重度狭窄,三尖瓣重度反流;心电图提示心房颤动;氨基末端脑钠肽前体(NT-proBNP)1371 ng/L。
入院后评估考虑外科再次瓣膜置换手术风险高,美国胸外科医师协会(Society of Thoracic Surgeons,STS)评分10.915%,同时患者也拒绝再次外科手术。经心脏瓣膜团队评估后,认为目前有再次二尖瓣置换手术指征,但患者高龄,且再次外科手术风险高,适合经导管微创二尖瓣置换手术(瓣中瓣)。国际上目前二尖瓣介入瓣中瓣(ViV)手术使用得最多的器械是 Edwards Sapien XT 和 SAPIEN 3 经导管瓣膜系统(Edwards),临床研究证据相对充分,故拟使用 SAPIEN 3 进行经股静脉房间隔途径二尖瓣瓣中瓣置换术(ViV-TMVR)。
瓣膜团队在术前对患者进行了详细的影像评估。术前超声心动图提示二尖瓣生物瓣增厚与运动减弱,平均跨瓣压差明显增加。心脏 CT 提示双心房及右心室增大,房间隔增厚,生物瓣瓣叶增厚主要位于瓣叶基底部,结合 CT 所测量数据和 Valve in Valve App(version 2.0,UBQO Limited,London,UK)[1] 的推荐,SAPIEN 3 的 23 mm 瓣膜适合该型号生物瓣的瓣中瓣植入。术前通过 CT 三维影像模拟植入23 mm SAPIEN 3 瓣膜,测得被部分遮挡的新左室流出道(Neo-LVOT)面积为 2.8 cm2,且自身二尖瓣前叶既往已经外科切除,左室流出道梗阻风险小。手术路径上,患者既往曾行房间隔修补,CT 提示房间隔增厚,术中可能存在穿刺房间隔困难及并发症风险增加,需经食管超声引导和准备电刀辅助穿刺。
ViV-TMVR 手术过程见图 1。患者插管全身麻醉,贴电刀电极片,颈内静脉放置 6F 鞘备用于临时起搏电极。放置食管超声探头,完成右心导管评估。食管超声引导下,定位穿刺针于房间隔后下份,因常规穿刺不能通过,使用电刀辅助完成房间隔穿刺。肝素化,钢丝进入左上肺静脉,导管测量左房压力。经左侧股动脉导入猪尾导管,左心导管评估及左室造影。使用 10 mm 球囊扩张房间隔穿刺部。使用眼镜蛇导管(Cobra)、超滑导丝跨狭窄的二尖瓣生物瓣,进入左心室,交换塑形的 Amplatzer 加硬导丝进入左室。预装载 SAPIEN 3 的 23 mm 瓣膜,确认瓣膜装载方向正确。沿轨道送入系统,以外科生物瓣瓣环切线位为投射角度,以原生物瓣金属环定位瓣膜,快速起搏 180 次/分,扩张瓣膜球囊,待球囊回缩后停起搏。术中即刻食管彩色超声提示平均跨瓣压为 8 mm Hg,采用 22 mm 非顺应性球囊(Atlas)14 ATM 进行后扩,再次超声评估平均跨瓣压为4 mm Hg。左室造影及彩超未见瓣周漏,左室流出道无梗阻,升主动脉压力 142/89 mm Hg,左室压力142/10 mmHg,撤出导丝及鞘管,结束手术。
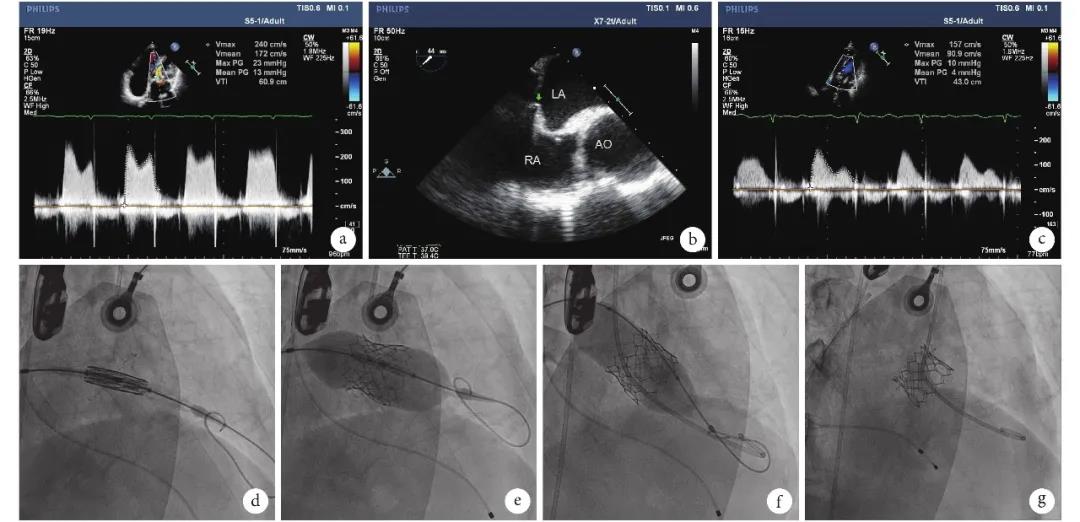
图1 手术前后超声心动图及手术瓣膜释放过程
a:术前彩二尖瓣压差 13 mm Hg;b:房间隔穿刺时,穿刺针在房间隔顶出的帐篷征,如箭头所示;c:最终术后二尖瓣压差 4 mmHg;d:瓣膜定位在原有二尖瓣生物瓣金属圈;e:球囊扩张释放瓣膜,瓣膜腰征明显;f:高压球囊后扩;g:瓣膜释放后最终状态
术后随访
患者术后 3 h 在 CCU 拔除气管插管,无气促等不适,术后第 1 d 转出监护室,第 3 d 出院。
讨 论
当二尖瓣生物瓣置换的患者出现瓣膜衰败导致心力衰竭加重,需再次换瓣手术时,面临二次外科开胸换瓣的手术风险明显增加。很多这类患者高龄,合并症多,会进一步增加外科手术风险。当外科高风险和存在外科禁忌时,经导管瓣中瓣植入被 2020 年 ACC/AHA 瓣膜性心脏病指南作为Ⅱ a 类推荐[2]。近年来,该项技术在国际上已有较多报道提示其安全性和有效性高,但在中国内地尚无临床应用报道[3-6]。本例患者高龄,外科风险高,STS 评分 10.915%,适合应用瓣中瓣技术进行经导管瓣膜置换手术。
经导管二尖瓣瓣中瓣介入手术从路径上有经心尖和经股静脉-房间隔两种术式。从目前研究报道来看,二尖瓣的瓣中瓣植入中,经心尖途径应用更早。但经股静脉路径的创伤小,在外科高危患者可能更具有低创伤和安全性优势。Frerker 等[3] 研究对比了股静脉途径和心尖途径在临床效果、并发症及远期生存率等。虽然手术成功率及并发症等两种途径无统计学差异,但经股静脉-房间隔途径有更高远期生存率。该患者高龄,合并症多,身体虚弱,但股静脉途径创伤小,术后康复快,患者清醒后就拔除了气管插管,气紧症状改善,监护室时间只有 1 d,术后第 3 d 就能出院。
该手术虽然创伤小,但手术过程仍然存在较多潜在风险,涉及的技术难点较多,需要多学科团队协作。二尖瓣进行瓣中瓣植入可能会导致左室流出道梗阻,这需要术前进行 CT 三维影像分析,模拟植入的新瓣膜可能在多个角度对左室流出道产生阻挡。该患者左室流出道相对较宽,室间隔没有明显增厚,且二尖瓣前叶已经切除,虽然主动脉瓣环和二尖瓣环成角较大,但经术前 CT 分析基本可以排除左室流出道明显梗阻风险。经股静脉途径需进行房间隔穿刺建立入路,为增加系统同轴性及操作空间,房间隔穿刺位点需尽量靠后下,这需要超声引导下穿刺,对术者和超声医生的协作要求较高。该患者既往曾行房间隔修补,房间隔有明显增厚,常规穿刺很难穿透房间隔或者不能精确穿刺,增加心脏穿孔等并发症。因此,术前准备了电刀,在常规穿刺失败后,穿刺针连接电刀辅助穿刺成功。该患者为狭窄性生物瓣衰败,左心室小,轨道稳定性下降,瓣膜系统通过难度增加,需小心仔细操作,防止系统通过失败。由于衰败瓣膜的组织增生,患者介入瓣膜释放以后,仍有较高跨瓣压差,我们按计划进行了高压球囊后扩。该型生物瓣膜(Biocor/Epic)经高压球囊后扩能增加瓣口面积,减少压差。但有些生物瓣进行后扩是无效的,因此术前必须得对原有生物瓣的型号进行了解,确定是否适合瓣中瓣、选择合适的方式和制定手术策略。
目前,国际上虽然有较多研究证实经导管的主动脉生物瓣 SAPIEN XT 和 SAPIEN 3 可安全有效的以瓣中瓣植入的方式置换衰败的二尖瓣生物瓣,但研究的规模仍较小,临床证据仍有空隙,因此 2020 瓣膜病指南仍只推荐瓣中瓣用于外科换瓣高风险或禁忌的患者。国内在该技术上仍处于起步阶段,对于有二尖瓣换瓣指征的低危患者,外科二尖瓣置换仍是首选策略。虽然二尖瓣介入治疗仍有较长的路要走,但随着微创介入技术的进步,器械的不断创新,二尖瓣瓣膜病治疗将继续走向微创化。
利益冲突:无。
作者贡献:魏家富负责施行手术、资料收集和撰写论文;陈飞资料收集、数据及 CT 影像分析;蒙炜负责施行手术、指导写作;魏薪超声检查和数据资料收集与分析;彭勇、李侨、何森、李怡坚、郑明霞、周轩、陈果负责施行手术;陈茂、冯沅负责施行手术、文稿审阅及经费支持,修改论文。
参考文献略。

请先登录,先评论.