氯吡格雷+PPI还能用吗?
来源: 发布时间:2009-05-27 09:19
氯吡格雷+PPI还能用吗? ——抗血小板药物暨抑酸药物合理应用研讨会报道
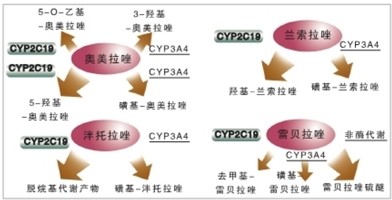
心血管内科、消化内科、临床药学专家共同解答 为了降低抗血小板治疗患者的消化道出血风险,加用质子泵抑制剂(PPI)似乎已成为临床常规,但今年初《加拿大医学会杂志》[CMAJ 2009,180(7):713]和《美国医学会杂志》[JAMA 2009,301(9):937]发表的两项大规模回顾性研究对这一用法提出了质疑 。两项研究均显示,氯吡格雷与PPI联用增加心血管事件发生风险。此后美国FDA也发出警告,提醒医生警惕以上两药联用的风险。 于是一石激起千层浪,临床医生开始困惑,还能将抗血小板药物与PPI联用吗?如果不用PPI,又有什么药可用来预防和处理消化道出血呢?……带着一系列疑问,本报于2009年5月6日在京组织召开了抗血小板药物暨抑酸药物合理应用研讨会,特邀心血管内科、消化内科与临床药学专家面对面,共同对以上问题答疑解惑,并期待对临床工作有所指导。 说现状 评研究 问题1 抗血小板治疗相关消化道出血现状如何? A高润霖 教授 抗血小板治疗出血风险值得关注 以阿司匹林一级、二级预防为例,其相关消化道大出血发生率为每千人0.19至1.6例。但由于用药人群基数大,用药时间长(通常为数十年),且患者发生消化道出血前往往无明显症状(阿司匹林所致溃疡一般无痛,经胃镜才能检出),故无法及时治疗。因而,消化道出血问题不容忽视。 B周玉杰 教授 氯吡格雷与阿司匹林出血风险相当 多项临床研究显示,氯吡格雷与阿司匹林的消化道出血风险几乎无差异。在氯吡格雷与阿司匹林预防缺血事件比较(CAPRIE)研究中,二者严重消化道出血发生率分别为0.52%和0.72%,差异仅为0.2%,无临床意义。2006年拉纳斯(Lanas)等的研究也显示,二者消化道出血风险相似。 C周丽雅 教授 氯吡格雷与阿司匹林的消化道损害机制不同 阿司匹林对消化道的损害是直接损伤黏膜,而氯吡格雷延缓溃疡愈合。部分患者使用阿司匹林发生消化道出血后,换用氯吡格雷仍有可能长期不再发生出血,但前提是既有的溃疡面已愈合。在阿司匹林所致溃疡尚未愈合前即贸然换用氯吡格雷存在安全性问题,可能引起溃疡迁延不愈。 D陈韵岱 教授 双联抗血小板治疗出血风险的院内统计资料少 关于抗血小板治疗相关消化道出血的发生率,国内资料很少,以个案报道为主。 回顾解放军总医院2008年1月至2009年3月收治的495例急性心肌梗死患者显示,在380例接受介入治疗并使用阿司匹林+氯吡格雷双联抗血小板治疗者中,住院期间发生上消化道出血者为4例(1.5%)。 问题2 近期发表的两项研究对临床影响如何?如何评价? A陈韵岱 教授 如果氯吡格雷不能与PPI联用,心血管医生将无所适从 2009年发表的几项研究,使心血管医生很茫然。血栓和消化道出血的高危因素有较多重叠,为临床选择抗血小板治疗方案带来一定困难。对于部分高危患者,如急性冠脉综合征(ACS)患者,有明确双联抗血小板治疗指征,既往较多使用PPI预防消化道出血。而近期PPI减弱氯吡格雷疗效的报道使心血管医生感到困惑,不知何药可用。此外,ACS患者用药较多,是否还有其他药物可能减弱抗血小板药物疗效,也将受关注。 B周玉杰 教授 可以用H2受体拮抗剂替代PPI吗? 在今年的两项研究发表前,我们多用PPI预防消化道溃疡,而研究发表后多采用H2受体拮抗剂替代PPI,因为研究显示雷尼替丁、法莫替丁等不影响氯吡格雷代谢,但其能否安全有效地防治抗血小板药物相关消化道不良反应还有待证实。另外,泮托拉唑对细胞色素P450(CYP)2C19的抑制作用也较小。关于抗血小板药物与PPI联用的问题,一项评价氯吡格雷、阿司匹林与PPI联用风险获益的随机研究(COGENT-1)正在进行,其结果预计今年12月公布,有望提供重要信息。 C高润霖 教授 无足够证据显示接受氯吡格雷者不能用PPI 目前,人们尚不清楚PPI与抗血小板药物的相互作用是否导致临床后果。现有前瞻性研究为小样本研究,一些提示PPI对氯吡格雷有影响,一些则提示无影响。近期发表的这两项显示氯吡格雷与PPI联用增加终点事件的研究都是回顾性研究,只能提出假设,不能作为结论。虽然美国FDA提出警示,但目前并无足够证据显示,接受双联抗血小板治疗或氯吡格雷单药治疗者不能使用PPI。近期,美国心血管造影与介入学会(SCAI)发表声明指出,ACS患者在接受心脏介入治疗后,需要继续接受氯吡格雷和其他抗血小板药物治疗,未经医生许可切勿擅自停药。SCAI同时建议医生遵从指南推荐,给接受心脏支架置入术的患者继续处方双联抗血小板药物,并根据患者个体情况酌情使用PPI。 D周丽雅 教授 氯吡格雷与PPI相互作用并无定论 关于氯吡格雷与PPI联合应用的现有文献中,支持两者可以或不能联用的各占一半,并无确定结论。如FAST-MI研究(注册研究)、3C研究(前瞻性队列研究)和CREDO研究(事后分析)均提示,PPI并不影响氯吡格雷疗效。 E张澍田 教授 发表于JAMA的研究有一定局限性 JAMA上发表的这项研究有一定局限性。首先,它是回顾性研究;其次,未考虑CYP多态性,不清楚白人、非裔或亚裔人群的情况有何不同;再次,该研究未进行分层分析,如所纳入人群的生活方式(吸烟、饮酒等)资料不详。因此,不能以此否定PPI,其结果只是给我们提出警示。 F林三仁 教授 不能断言氯吡格雷与PPI能或不能联用 基于当前研究结果相互矛盾的现状及临床实际情况,心血管医生能做的是,在给予患者氯吡格雷联合PPI治疗时,高度关注两药联用时的药效,不能绝对地说两药能或不能联用,不能把治疗的路完全堵死。 G王汝龙 教授 基因多态性影响氯吡格雷代谢 氯吡格雷经CYP2C19等代谢,代谢酶的基因多态性对氯吡格雷的药理学及临床药效学都有影响。CYP2C19的基因多态性发生率有人群差异,白人约30%,黑人约40%,东亚人约55%。在氯吡格雷治疗者中,携带功能降低CYP2C19等位基因的患者,血浆氯吡格雷活性代谢产物水平和血小板抑制作用显著降低,主要不良心血管事件(包括支架置入术后血栓形成)发生率升高。而通过检测基因多态性,可识别出这些患者。 氯吡格雷与PPI的多代谢途径 除CYP2C19外,氯吡格雷还可通过CYP3A4/5、CYP2B6、CYP1A2/1代谢。而对于PPI,不同药物存在差异,同种药物也有多种代谢途径(图1)。 H胡晋红 教授 不能简单禁止氯吡格雷与PPI联用 氯吡格雷与PPI的代谢通道有一致之处,关注两药联用时可能出现的问题非常重要。但两药的代谢途径不止一条,因而不能简单地禁止两药联用,应更多关注药物用量及疗效,并加强药物使用中的监测。图1 PPI的多代谢途径
找证据 寻对策 问题1 如何预防抗血小板药物引起的消化道出血? ——严把适应证—— A高润霖 教授 严格掌握抗血小板治疗适应证 使用阿司匹林进行心血管疾病一级预防需权衡患者获益和风险,只有获益远大于风险的人群才适用。指南推荐,10年心血管疾病风险>6%~10%的人群应使用阿司匹林。对于二级预防,阿司匹林减少死亡和再发心肌梗死的作用已被证实,所有无禁忌证者均需使用。若患者对阿司匹林过敏,用氯吡格雷替代。 ACS患者一般都须使用双联抗血小板治疗。①对于未置入支架者,研究提示1年双联抗血小板治疗的疗效优于1个月,一旦发生出血,可根据出血情况调整疗程。②对于置入裸金属支架(BMS)者,支架置入后1个月左右内皮愈合,使用双联抗血小板治疗1个月即可。③对于置入药物洗脱支架(DES)者,因内皮愈合时间延长,专家共识明确指出须使用双联抗血小板治疗至少1年。 B林三仁 教授 对接受抗血小板治疗者进行出血危险分层 要合理应用PPI,首先应区分出血高、低危人群,即通过评估患者接受抗血小板治疗后消化道出血发生危险,决定该用PPI、H2受体拮抗剂还是胃黏膜保护剂。 C周丽雅 教授 识别出血高危因素 年龄>65岁、有溃疡或消化道出血史、存在幽门螺杆菌(Hp)感染,阿司匹林剂量较大或接受双联抗血小板治疗,合用抗凝药、非类固醇类抗炎药(NSAID)等都是消化道出血高危因素。应积极治疗可纠正因素,如Hp感染。 D周玉杰 教授 CRUSADE出血评分可参考 《循环》杂志新近发表的一项研究使用了CRUSADE出血评分评价抗血小板治疗者的出血危险(表1),可供参考。E张澍田 教授 重视用药期间出血监测 在患者使用抗血小板药物(即使小剂量)期间,须监测消化道出血情况。①嘱患者观察便色,识别柏油样便;②检查便潜血,建议每次复诊时检查;③检测血常规,如每月1次,观察血红蛋白是否有下降趋势。若结果提示疑似出血或有出血征象,可行胃镜检查,以便早期诊治。 F林三仁 教授 H2受体拮抗剂、胃黏膜保护剂与PPI作用比较与选择 现有资料显示,H2受体拮抗剂预防消化道出血并发症作用逊于PPI,但不排除其有一定疗效。 胃黏膜保护剂为非损伤性药物,较安全,可长期应用。新近研究显示,瑞巴派特在预防NSAID(含阿司匹林)相关消化道症状方面有效,但效果远不如PPI。此外,对替普瑞酮也有大样本研究,但为回顾性,参考价值不高。总之,胃黏膜保护剂对消化道出血的预防有一定疗效,非高危人群长期应用抗血小板药物时可考虑适当加用。 可有效预防消化道出血的药物还是PPI,接受抗血小板治疗的出血高危人群仍需用PPI。针对氯吡格雷的代谢途径,理论上联用雷贝拉唑效果最好,因后者不主要经CYP2C19 和CYP3A4代谢,但尚缺乏证据。有研究显示,联用泮托拉唑效果较好。 间断使用PPI 目前临床医生面临的关键问题是,能否将PPI作为预防用药长期使用。从消化科医生的角度,反对患者长期服用PPI。若患者无泌酸问题,只因服用抗血小板药物而长期应用PPI,会导致胃酸功能全部被抑制,胃蛋白酶活性丧失,胃肠功能紊乱。因此,可采取间断服用PPI的方式,选择合理用药间期,即按需服用。例如,在介入治疗后前3个月(胃肠道反应高发期)服用PPI,之后停用,采用胃黏膜保护剂替代,若有任何胃肠不适,再应用PPI。 G高润霖 教授 高危患者仍需使用PPI 出血危险高的患者仍需使用PPI,但不必长期用,如急性心肌梗死患者接受支架置入,在双联抗血小板治疗同时仍应输注奥美拉唑,之后改为口服。 H陈韵岱 教授 短期使用PPI或可行 具体分析JAMA上发表的这项2年期回顾性研究结果可见,在前半年,接受氯吡格雷+PPI治疗者的心血管事件发生率并未增加,即使在1年时也只有很小差异。尽管并无临床证据显示前3个月使用PPI对后期氯吡格雷治疗有无影响,但使用3个月PPI后停药恢复也是一个办法。 I张澍田 教授 H2受体拮抗剂亦可使用 在双联抗血小板治疗基础上使用H2受体拮抗剂,不存在禁忌证。H2受体拮抗剂的抑酸效果不如PPI,但不影响氯吡格雷代谢,从此角度讲,权衡风险和效益,在患者不用PPI时(意味着无任何措施预防消化道出血),不如联用H2受体拮抗剂。可选择效果最好且对氯吡格雷代谢影响最小的药物,如法莫替丁。对于农村地区人群,H2受体拮抗剂也较适用。 表1 CRUSADE出血评分 评分结果说明如下: ≤20分:极低危(出血率为3.1%) 21~30分:低危(出血率为5.5%) 31~40分:中危(出血率为8.6%) 41~50分:高危(出血率为11.9%) >50分:极高危(出血率为19.5%) 问题2 患者发生消化道出血时,如何处理? A高润霖 教授 权衡利弊,选择性停用抗血小板治疗 接受抗血小板药物一、二级预防者发生消化道出血时,可暂停抗血小板药物并进行相应处理;未置入支架的ACS患者发生消化道出血时,即使抗血小板治疗未达1年,也可视情况停用1种或2种抗血小板药物;置入支架的ACS患者在接受双联抗血小板治疗期间发生消化道出血时,若停用抗血小板药物,易发生支架内血栓,死亡风险很高,权衡风险获益,不能只依赖停药,而应对出血进行急诊局部处理。 B张澍田 教授 高危人群可在不停用双联抗血小板治疗的情况下处理出血 对于接受双联抗血小板治疗+PPI时发生消化道出血的患者,权衡再发心血管事件和出血风险,可不停用抗血小板治疗,积极对出血部位进行局部处理(如内镜下止血)。 三方初步共识 通过心血管内科、消化内科与临床药学专家的共同讨论,初步对抗血小板药物与抑酸药物的使用达成以下共识: 1. 严格掌握抗血小板治疗适应证 对于一级预防,患者需长期使用抗血小板药物,应严格评估风险与益处。对于二级预防,所有无禁忌证者均需使用阿司匹林,若患者存在阿司匹林过敏,应用氯吡格雷替代。但是,对于慢性稳定性心绞痛的二级预防,不主张使用双联抗血小板治疗。 对于ACS患者,未置入支架和置入BMS者所需双联抗血小板治疗时间较短,但置入DES者须接受至少1年双联抗血小板治疗。心血管医生在选择治疗方式时,需结合心脏评估和消化道对双联抗血小板治疗耐受力评估结果,很好地权衡利弊。 2. 识别高危患者,“按需”使用PPI 对于必须接受抗血小板治疗的患者,需进一步评估其消化道出血发生危险,区分高危和非高危患者。 对于高危患者,“按需(间断或必要时)”使用PPI。如在使用抗血小板药物最初3个月内使用PPI。对于与氯吡格雷联用时PPI的选择,理论上雷贝拉唑最佳,但需循证证据证实。现有研究提示泮托拉唑效果较好。 对于非高危患者,以及高危患者在停用PPI间期,可使用黏膜保护剂(如瑞巴派特)、H2受体拮抗剂(如法莫替丁)。 3. 对使用抗血小板治疗的患者进行出血监测 对所有接受抗血小板治疗者,都需进行出血监测,及早发现出血迹象。监测项目包括便潜血和血常规,必要时行内镜检查。一旦发现患者有出血迹象,加用PPI,继续密切监测,若仍有出血,需积极处理(如停用抗血小板药物或内镜干预)。 鉴于目前关于氯吡格雷与PPI合用是否降低氯吡格雷疗效的研究结果不一致,尚不能对此问题定论。根据具体临床情况,氯吡格雷与PPI仍需联用,但临床医生应提高警惕,同时继续关注新的研究结果。 来源:中国医学论坛报

请先登录,先评论.