RAAS(血管紧张素-肾素-醛固酮系统与心房颤动的关系研究
来源:医心网 发布时间:2005-11-01 09:22
北京友谊医院心血管疾病诊治研究中心 邢云利
中文摘要
背景:随着人口老龄化的加剧,房颤的发生率,致残、致死率逐年增加。目前房颤发生机制尚不清楚,治疗效果不佳。研究表明心房重构,特别是结构重构是房颤发生、发展和复发的基质。其病理表现为心房的肥厚、扩大及纤维化,影响心脏传导和不应期,促进房颤的发生和维持,是近年研究的热点。流行病学、临床和基础研究提示炎症可能与心房的结构重构相关。我中心曾入选42例患者进行研究,发现慢性房颤患者血浆RAAS各组分较窦性心律明显升高,并与左房直径正相关。本研究进一步扩大样本量,评估RAAS对心房结构重构以及房颤发生的影响。方法和结果:入选97例患者,将其分为窦性心律组(SR,n=31),阵发房颤组(PAF,n=34)和持续房颤组(CAF,n=32)。比较各组血浆肾素,血管紧张素II以及醛固酮水平,及其与左房直径的关系。结果显示CAF组患者平均左房直径与SR组和PAF组相比均明显增大(p<0.01),血浆肾素、AngⅡ、Ald浓度较SR组明显升高(p<0.05)。左心房直径与血浆RAAS各组分有明显正相关关系(p<0.05)。结论: 肾素-血管紧张素-醛固酮系统(RAAS)可能参与了房颤心房结构重构。关键词:房颤,结构重构,血管紧张素-肾素-醛固酮系统,左心房直径
Research on the relationship between RAAS (renin- angiotension-aldosterone system) and atrial fibrillation
Abstract
Background:In the aging society, the mobility and mortality of atrial fibrillation increase. However,the machanism of atrial fibrillation are still unclear.and the therapy are not efficient. It is well known that atrial remodeling ,especially structural remodeling is the basis of occurrence 、development and recurrence of atrial fibrillation .It mainly shows the enlargement and fibrosis of myocardia, affecting conduction and refractory period. Structual remodeling accelerates the occurrence and maintenance of atrial fibrillation ,and is regarded as current research hotspots. From the points of epidemiological, clinical and basic research, inflammation may involve the structural remodeling. So comparing renin-angiotensio、aldosterone and left atria diameter between atrial fibrillation and sinus rhythm, paroxysmal and persistent fibrillation , our study try to know the effects of inflammation on structural remodeling and atrial fibrillation. Methods and Results:Enrolled 97 patients were divided into three groups: sinus rhythm group (SR,n=31), paroxysmal atrial fibrillation (PAF,n=34), and chronic atrial fibrillation group (CAF,n=32).Compare renin-angiotensio、aldosterone and left atria diameter in different groups and know the relationship between them. The results show that renin-angiotensio、aldosterone and left atria diameter in patients with CAF increase significantly than SR and PAF (P>0.05). There is a positive relationship between them. Conclusions: Maybe RAAS involve the structural remodeling of left atrium , accelerating the occurrence and development of atrial fibrillation. Key Words: atrial fibrillation,structual remodeling, RAAS, left atria diameter
背 景
心房颤动(简称房颤)是指心房的不规则颤动,可以诱发心功能不全,脑卒中以及外周血管栓塞。随着人口老龄化的加剧,房颤的发生率,致残、致死率逐年增加。流行病调查显示人群总体房颤发生率为1%,50岁以上患者房颤发病率为6.5%,80岁以上患者发病率为30%。目前治疗房颤的方法如药物、电转复、射频消融术以及手术效果均不理想。房颤的发生机制尚不清楚。
研究表明心房重构是房颤发生和发展的核心环节。它包括电重构、收缩功能重构以及结构重构。电重构和收缩功能重构出现早,持续时间短,房颤转复后可以恢复;而结构重构主要为心房肌肥厚、扩大、纤维化等形态学变化,一方面形成许多折返子波,直接影响心房肌不应期和传导,另一方面心房增大慢性牵拉周围心肌细胞,刺激细胞内信号传导系统,进一步促使房颤维持。因此研究心房结构重构的机制,可以帮助我们了解房颤发展和复发的机理,从根本上防治房颤。
流行病学、临床以及基础研究显示血管紧张素-肾素-醛固酮系统(RAAS)激活可能参与了心房的结构重构,并且愈来愈多的基础和临床研究为这种设想提供了有力证据:1)流行病学调查证实,心衰患者的房颤发生率达50%以上,心衰越重,房颤的发生率越高;2)阻断肾素-血管紧张素-醛固酮系统(卡托普利,缬沙坦)可以减轻犬心房颤动模型的心房电重构,减轻心房有效不应期缩短,而且依那普利还可通过作用于血管紧张素II发挥效应的信号传导系统(ERK),降低心房传导的异源性,减轻心房肌纤维化,防止心房结构重构;3)TRACE研究中,应用Trandolapril 4年随访可使伴左室功能低下病人的心房颤动发生率降低达55%。所有这些研究结果均提示,肾素-血管紧张素系统和交感神经系统可能在心房颤动的核心环节一心房结构重构的发生中起着重要作用。本研究比较各类房颤患者体内的肾素-血管紧张素、醛固酮水平,探索RAAS在房颤发生、发展以及持续中的作用。
资料与方法
一 患者人群与分组
研究对象为2002年10月到2003年11月因心脏疾患住院的患者,共97例(包括窦性心律31例,房颤心律66例),年龄61.9±11.5岁。病因包括孤立性、高血压、冠心病和瓣膜病(风湿性心脏病和先天性心脏病)。若患者同时患有高血压和冠心病,结合超声情况,若室壁运动减弱,心室腔明显增大,则考虑为冠心病引起的房颤。同样,若瓣膜疾病伴有其他可以引起心房重塑的疾病,结合病史、超声结果做出判断。
入选患者分为窦性心律组(SR),31例;阵发房颤(PAF),34例;持续房颤组(CAF),32例。入选标准:1)窦性心律组定义为心电图显示窦性心律;阵发房颤组定义为房颤发作不超过7天,且可自行终止。持续房颤组为房颤发作超过7天,不能自行终止,多由电复律或药物转复。2)心脏功能Ⅰ级(NYHA分级),心脏超声示左室射血分数>50%。3)正在服用ACE抑制剂或AR-B等药物的患者停药至少2周。术前行心脏超声、常规化验、心电图、甲状腺功能测定、肾功能检查等排除充血性心力衰竭、甲亢、肾脏疾病、神经系统疾病等。
二 标本测量
1 肾素、血管紧张素II、醛固酮的测定
清晨空腹静卧1小时后采集肘前静脉血5毫升,立即送至北京友谊医院放免实验室,操作方法按试剂说明书进行。
放免试剂盒由中国同位素公司北方免疫试剂研究所提供。
采用HP5500多普勒超声仪,以心脏长轴M型切面测量的左心房前后径作为心房结构重构的指标。
三 统计分析
所测得的数据以均数±SD表示。两样本构成本的比较用χ2检验,两样本均数的比较采用t检验。多个样本均数的比较采用单因素方差分析(ONE-WAY ANOVA)。采用直线回归分析两变量之间的相关关系。p<0.05被认为有统计学意义,P<0.01有显著统计学差异。本研究使用SPSS 10.0软件进行统计学数据处理。
结 果
一 患者临床特征
该试验入选97例患者,年龄61.9±11.5岁,分为窦性心律组(n=31),阵发房颤组(n=34),持续房颤组(n=32)。男性48例(49.5%),女性49例(50.5%)。孤立性房颤21例(31.8%),高血压房颤17例(25.8%),瓣膜病(包括风湿性心脏病和先天性心脏病)引起的16例(24.2%),冠心病房颤16例(24.2%)。临床特征,如年龄、性别、伴随疾病构成比,均无统计学上的显著差异性(P>0.05)。(见表1、2)
表1正常组和房颤组患者的临床特点
|
分组
病例数 |
正常对照组(n=31) |
房颤组(n=66) |
| 年龄,岁 | 64.9 | 65.1 |
| 男性,n(%) | 11(61.1) | 37(52.9) |
| 高血压, n(%) | 8(25.8) | 17(25.8) |
| 冠心病,n(%) | 7(22.6) | 16(24.2) |
| 瓣膜病,n(%) | 7(22.6) | 16(24.2) |
| 孤立性,n(%) | 9(29.0) | 21(31.8) |
表2 阵发房颤组和持续房颤组临床特点
|
分组 病例数 |
正常对照组(n=31) |
阵发房颤组(n=34) |
持续房颤组(n=32) |
| 年龄,岁 | 64.9 | 64.2 | 64.6 |
| 男性,n(%) | 11(61.1) | 11(52.4) | 17(53.1) |
| 高血压, n(%) | 8(25.8) | 8(23.5) | 8(25.0) |
| 冠心病,n(%) | 7(22.6) | 8(23.5) | 8(25.0) |
| 瓣膜病,n(%) | 7(22.6) | 7(20.6) | 7(21.9) |
| 孤立性,n(%) | 9(29.0) | 11(32.4) | 9(28.1) |
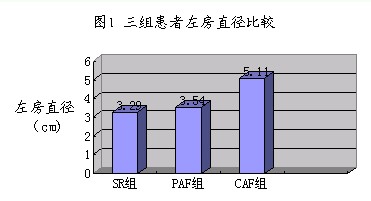
二 不同组别之间的左房大小比较(见图1 )
对照组左心房直径3.29±0.38cm, 阵发房颤组为3.54±0.65cm,持续房颤组5.11±1.11cm。
由图中可以看出,CAF组患者平均左心房直径明显增加,P=0.000〈0.01;与SR组患者相比增大了55.3%,与PAF相比增大了44.4%。PAF组与SR相比,平均左房直径有增大趋势(增加7.6%),但没有显著差异,P=0.08>0.05。
三 不同组别的血浆肾素、angⅡ、Ald水平(见表3、图2)
肾素(ng/ml·h)
angⅡ(pg/ml)
Ald (pg/ml)
SR组
0.48±0.14
51.51±25.88
271.89±77.77
PAF组
0.58±0.21
70.05±31.83
299.27±81.48
CAF组
0.88±0.53
113.16±68.24
365.00±105.26
表3为患者的肾素、angⅡ、Ald水平。图1用柱形图对三者的测量结果进行比较。可以看出CAF组的血浆肾素、AngⅡ、Ald浓度明显高于SR组(分别升高83.3%、61.7%、34.2%,p<0.05)。PAF组和SR组,CAF组和PAF组之间的血浆AngⅡ、Ald浓度虽然升高,但没有显著差异(p>0.05)。但CAF组血浆肾素浓度明显高于pAF组(升高51.7%,p<0.05)。
表3 三组病人的血浆肾素、angⅡ、Ald水平
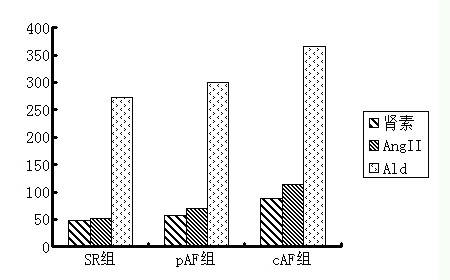
、图 2三组病人循环血浆肾素、血管紧张素、醛固酮水平比较
二 左心房直径与血浆RAAS各组分的关系(见图3)
图3为三组病人的左心房直径与循环血浆肾素、AngⅡ、Ald水平所作的相关统计学分析,结果提示两者存在有明显的正相关(p<0.05)。其中肾素水平与左心房直径相关性最强(p<0.01),其次是Ald(p=0.042)和AngⅡ(p=0.048)。
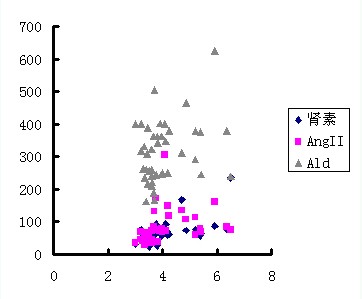
图 3 三组病人左心房直径与肾素、AngII、Ald之间关系的散点图
(图中横坐标为左心房直径,纵坐标为肾素、AngⅡ、Ald的相对值)
讨 论
心房纤颤是临床上常见的房性心律失常。研究表明心房重构,特别是结构重塑在房颤的发生和持续中起了重要作用。鉴于持续房颤患者的心房肌细胞与心室肌缺血(冬眠心肌)在病理特征方面有极大的相似性,我们推测神经内分泌因素如肾素-血管紧张素-醛固酮系统在促使心房肌细胞肥厚、纤维化,体积增大(即结构重构)方面发挥着一定作用。该研究基本证实了这一点。
首先,CAF患者左心房直径较其他两组明显增大,PAF与SR相比虽有增大的趋势,但没有统计学差异。说明房颤持续时间越长,心房结构重构越明显。
其次,CAF患者循环血浆中肾素、AngⅡ、Ald水平明显升高,与SR组相比有显著差异。可能与下列因素有关:(1)心悸、胸闷等不适症状引起交感神经兴奋性增加,未梢释放大量儿茶酚胺递质,促进肾素的分泌和AngⅡ的生成;(2)房颤时心房有效收缩丧失,左心室充盈降低,心排血量减少,从而使肾血管有效灌注压降低,肾素分泌增加。
最后,左心房直径与循环血浆肾素、AngⅡ、Ald水平呈明显正相关,提示血浆肾素、AngⅡ、Ald对左心房结构产生了一定影响,导致结构重构的形成和心房纤颤的持续。可能的机制有:首先,AngⅡ等及其引起的交感神经兴奋,使心房激动的频率增加,产生频率诱导性结构重构;其二,AngⅡ等通过收缩冠状动脉,增强血管平滑肌对缩血管物质的敏感性,加重心房肌缺血,促使心房肌纤维化。其三,AngⅡ等还可增加细胞内Ca2+超载,加剧心房的电重构和收缩功能重构。其四,AngⅡ等直接作用于心房肌,介导心房肌细胞增生和间质纤维化。
试验局限性
首先,由于临床资料的限制,本研究未能明确心房颤动发生时右心房的情况。推测就象心室重构主要发生在左心室一样,心脏功能活动时,特别是在病理状态下,左心房的血液动力学改变通常较右心房更明显。
其次,本研究心房肌结构重构主要以超声心动图测量的左心房直径来评价,缺乏病理解剖等更精确的指标。测量循环,而不是心房肌组织肾素、血管紧张素、醛固酮、hs-CRP以及ET-1,只能间接反映心房肌的物质浓度。
再次,因是临床研究,可能存在一些不可预知的影响因素,然而三组患者入选标准一致,构成比基本均衡,具有可比性。
最后,试验样本量相对少,尚需进一步扩大样本量。
参考文献:
1.Sato A, Liu JP, Funder JW. Aldosterone rapidly represses proteinkinase C activity in neonatal rat cardiomyocytes in vitro. Endocrinology 1997;138: 3410-3416.
2.龚素珍, 刘培庆, 鲁伟,等.醛固酮对心室成纤维细胞分泌内皮素的影响.生理学报 2001;53(1):23-26.
3.Shinagawa K,Miitamura H,Ogawa,S,et al.Effects of inhibiting Na+/H+-exchange or angiotensin converting enzyme on atrial tachycardia-induced remodeling. Cardiovasc Res 2002;54:438-446.
4.Nakashima H,Kumagai K,Urata H,et al.Angiotensin Ⅱ antagonist prevents electrical remodeling in atrial fibrillation.Circulation 2000;101:2612-2617.
5.Wijffels MC,Kirchhof CJ,Dorland R,et al.Electrical remodeling due to atrial fibrillation in chronically instrumented conscious goats:roles of neurohumoral changes,ischemia,atrial stretch,and high rate of electrical activation.Circulation 1997;96:3710-3720.

请先登录,先评论.