专题∣同品种医疗器械的评价方法
发布于:2015-07-07 09:50
今天,我们为大家梳理通过同品种医疗器械临床数据进行分析评价的方法与路径。
我们将“同品种医疗器械评价”拆分为定义、评价路径、对比项目和判定方法4个部分:


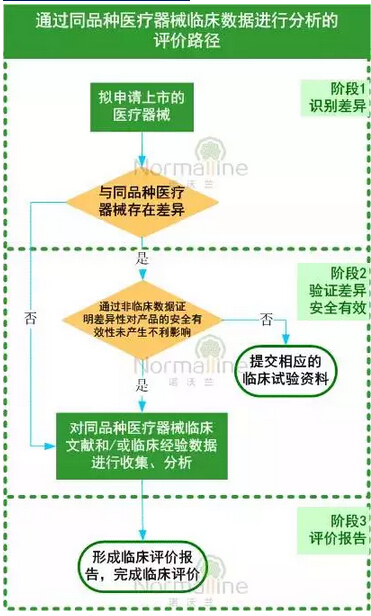
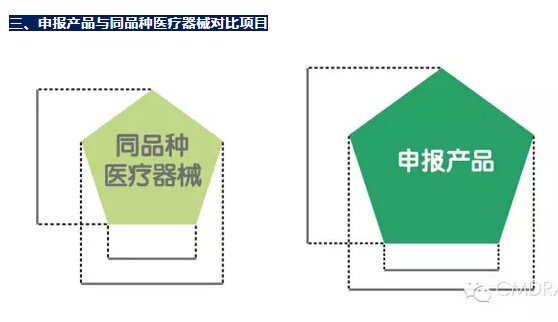
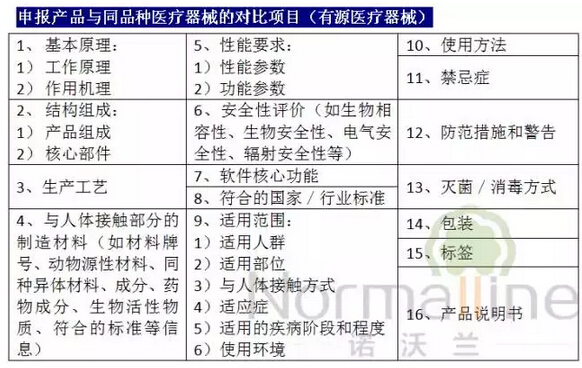
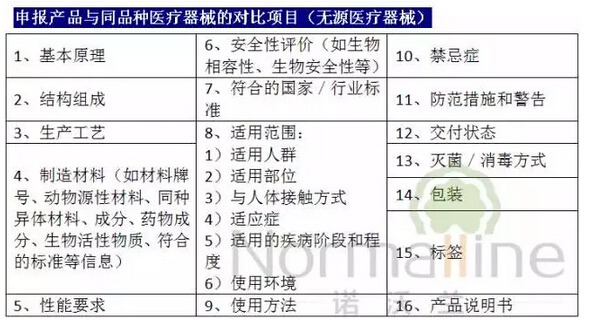

1)对比内容包括定性和定量数据、验证和确认结果;
2)应详述申报产品与同品种医疗器械的相同性和差异性;

3)对差异性是否对产品的安全有效性产生不利影响,应通过申报产品自身的数据进行验证和/或确认,如申报产品的非临床研究数据、临床文献数据、临床经验数据、针对差异性在中国境内开展的临床试验的数据;
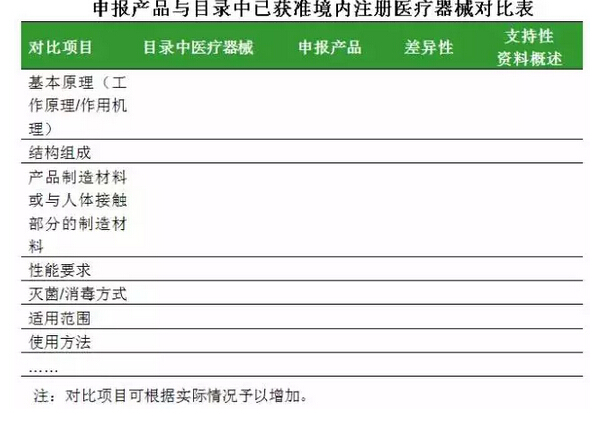
4)注册申请人应以列表形式提供对比信息。若存在不适用的项目,应说明不适用的理由。
转自:CMDRA
相关文章:



 京公网安备 11010102002968号
京公网安备 11010102002968号