ACS患者抗血小板定制治疗的机制与时机
发布于:2016-07-18 09:39
2016年6月,第九届齐鲁胸痛论坛冠心病介入诊疗技术培训提高班在济南召开。会上,来自兰州大学第一医院心内科的王志禄教授做了题为“ACS患者抗血小板定制治疗的机制与时机”的精彩报告。
一、P2Y12受体的作用机制
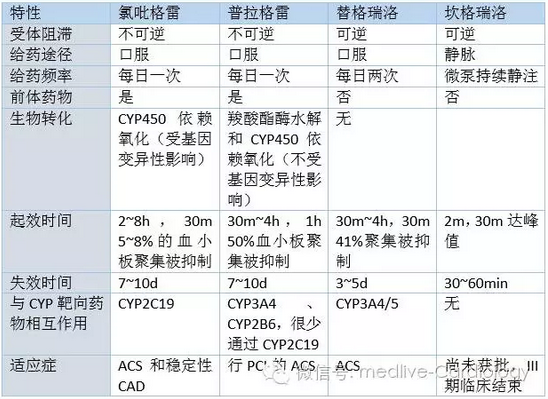
二、氯吡格雷抵抗综合征
双抗治疗(DAPT)是ACS治疗的基石,作为其标准化治疗已应用10多年。当DAPT降低ACS死亡率时,一些患者经历了再发血栓事件,特别是因ACS行PCI的患者处于支架血栓风险之中,所有ACS患者,无论血管重建状态,都具有再发心血管事件的风险。
氯吡格雷抵抗最佳定义是指难以抑制其靶目标的活性(如P2Y12R)。临床上,使用抗血小板药物的负荷量后,对血小板抑制应答不良,血小板活性增加,持续聚集数小时,被描述为治疗后的血小板高反应性(HTPR),而且与心血管死亡风险升高3.4倍、支架血栓风险升高4倍有关。
氯吡格雷抵抗关注于氯吡格雷对血小板活性的抑制情况,是用药前后的血小板功能指标的绝对值,理论上能更好的反映患者治疗当前的血栓风险。尽管氯吡格雷不能抑制P2Y12R的最常见原因是医疗非依从性的,应答氯吡格雷的个体化差异却集中在HTPR。基因多态性、药物与药物之间的相互作用、饮食、吸烟、糖尿病、肥胖和慢性肾脏疾病都可能引发HTPR。
三、ACS患者基因型和表型定向的药物治疗方法
在涉及氯吡格雷代谢的众多CYP450酶系统中,CYP2C19基因多态性显著影响氯吡格雷的应答。其中,大约15%的白人和非洲人以及30%的亚洲人被认为涉及CYP2C19*2功能缺失基因多态性,尽管有报道在白种人中高达30%和东亚人群占50%。至少存在1个CYP2C19*2等位基因的量可降低氯吡格雷活化代谢水平,从而降低血小板聚集抑制。
2010年,FDA第三次发布黑框警告,警示氯吡格雷的使用风险,建议服用氯吡格雷的患者做CYP2C19基因检测。警告指出,根据患者CYP2C19基因型,特别是其中包含功能减低等位基因的2个CYP2C19的患者,氯吡格雷在个体中有降低疗效的作用,但未评价这些结果如何影响治疗。此外,也不存在关于降低药物应答所导致弱化临床心血管预后和出现1~2个功能等位基因缺失如何影响这些临床预后的共识。
2010年发表于《JAMA》的一项meta分析显示,1个及2个功能减低CYP2C19变异体携带者主要不良心血管预后风险增加;1个功能减低等位基因(杂合子)与2个功能减低等位基因(纯合子)增加支架血栓危险。PLATO基因亚组研究显示,携带者(无功能突变等位基因缺失的例数)与非携带者比较,采用氯吡格雷治疗30天其心血管死亡、心肌梗死或卒中发生率存在明显差异,但未持续12个月。CHARISMA基因研究发现,接受PCI的少数患者,CYP2C19*2功能减低等位基因携带者无差异。
2013年CPIC指南认为,患者和临床特点可能影响采用与基因型状态一致的DAPT治疗患者的心血管预后。接受PCI治疗的亚组更多的受到了基因药理学疗效的影响。相反,予以药物治疗而未行PCI的ACS患者并未出现不良的临床预后。2012 ACCF/AHA不稳定心绞痛-非ST段抬高心肌梗死患者管理指南指出,以病例为基础,对于CYP2C19功能缺失等位基因的患者应考虑基因检测,特别注意那些尽管采用氯吡格雷治疗的ACS患者。2013年CPIC指南还建议,基于基因型优化抗血小板治疗,但未就实施基因型检测进行评论。
血小板治疗高反应性的监测
血小板反应性的基因表现分析为评估使用氯吡格雷治疗患者不良心血管事件提供了一个可选择的方法。目前HTPR监测有多种方法可供选择,例如光比浊法、血管扩张刺激磷蛋白磷酸化测定、阻抗法、即时诊断。多项研究凸显了HTPR和不良心血管临床预后的预期关系。Meta分析显示,一级终点高发率常发生于PRU值高四分位数,提示PRU潜在界值在230可描述HTPR。
表型定向治疗
鉴于HTPR的预后意义,有必要使用血小板反应性的表型分析法定制ACS的抗血小板治疗方案,主要作为剂量的改变或更换、替代抗血小板药物,以努力影响临床结果。然而,大量设计良好的研究结果喜忧参半,限制了对这种方法的研究热情。
GRAVITAS研究:高剂量氯吡格雷维持组HTPR患者30天血小板反应性显著降低,而6月一级终点无差异。重要的是,该研究尽管招募了大量患者,但研究事件率很低,可能遭受了统计力量的不足。GRAVITAS研究事后析因分析:血小板反应性可能是动态变化的,随着PCI术后时间的推移可能需要系列的血小板反应性预期值去指导治疗。
ADAPT-DES研究发现,PRU>并非死亡的独立预测因子,可能系血栓和出血的竞争结果。采用PRU>208和>230两个界值显示HTPR,结果表明HTPR和确定或可能的支架血栓显著相关,HTPR组患者临床相关出血显著降低。
TRIGGER-PCI研究:评估服用氯吡格雷期间选择性PCI术后伴HTPR患者,进行普拉格雷与氯吡格雷转换的有效性、安全性和抗血小板疗效,试验因继发低的初发事件而提前终止。其原因可能与低的VerifyNow PRU界值和低危患者相关,更与常用的二代DES支架有关。
ARCTIC临床试验:与未检测的标准抗血小板治疗组比较,根据床旁血小板功能检测调整冠脉支架患者的抗血小板治疗方案,其临床预后未见显著改善。
使用氯吡格雷治疗期间的HTPR患者,在与普拉格雷转换或氯吡格雷加量及采用其他噻吩砒啶药物治疗期间血小板低反应性患者,被定义为超过90%的血小板抑制,即改用氯吡格雷治疗或维持。在HTPR检测界值和异质性方面缺乏共识时,干预(剂量/药物变化)可能导致零的结果。
TRILOGY-ACS试验亚组分析显示,普拉格雷可显著降低HTPR,但并未相应减少30天心血管相关死亡率、非致死性心肌梗死或卒中。
氯吡格雷治疗无应答,以表型指导使用替格瑞洛的研究初步结果显示:与标准剂量氯吡格雷比较,仅仅见到采用高剂量氯吡格雷和普拉格雷及替格瑞洛治疗的患者显示与更大的血小板抑制相关。然而,仍旧缺乏评估氯吡格雷无应答者改换替格瑞洛治疗对预后影响的评估试验。
鉴于上述不确定的结果,使用指南规范血小板功能检测的态度是宽泛的。2011 ACCF/AHA/SCAI和2011ESC分别对PCI术后和接受PCI术的NSTEMI-ACS等使用抗血小板药物时检测血小板功能的问题作出解释。2011 ACCF/AHA/SCAI的PCI指南建议,在PCI术后考虑有临床预后不良高危风险的患者中和如果结果显示存在HTPR,考虑使用普拉格雷或替格瑞洛的患者可考虑血小板功能检测。同样,2011ESC NSTEMI-ACS指南认为血小板功能检测系IIb类适应证,在正在使用氯吡格雷的特殊病例中可进行血小板功能检测。
总结
1、目前ACS的DAPT治疗的成功,部分意义上讲,取决于对P2Y12R的抑制成功
2、准确评价血小板抑制剂在患者管理中的疗效可能有着重要的作用
3、研究表明,HTPR授予更为严重的缺血预后风险,由此可能促使治疗选择的评价,特别是经历反复心血管事件的患者。
4、证据支持使用普拉格雷和替格瑞洛以替代因反复心血管事件高发风险和低危出血性ACS患者治疗中的氯吡格雷。
5、基因型评估在确定个体化治疗中也可能起着潜在作用。
6、鉴于上述在改善心血管预后与基因型或表型指导治疗紧密相关的证据,在临床上常规使用CYP2C19基因多态性和血小板反应性检测尚不清楚。
7、尽管现有一些有前途的数据,而应用新的抗血小板药物时仍需设计良好的RCT以评估个体基因型或表型导向治疗的临床影响。
8、进一步,ACS急诊情况下,静脉配方的抗血小板药物的概念还是有趣的,更多的工作是有必要去定义ACS治疗中这些药物的潜在作用。
9、更好地了解血小板活化和随后抑制的遗传与表型之间的复杂作用是极为重要的,作为医学实践可继续向患者提供个性化的服务。
转自:医脉通心血管
责编:Sami



 京公网安备 11010102002968号
京公网安备 11010102002968号