国内首例经皮肺动脉瓣置入术
发布于:2013-09-10 16:15
文/ 潘文志 周达新 葛均波 复旦大学附属中山医院
只能爬2~3层楼。
体检:BP 106/70mmHg,颈静脉不充盈,双肺呼吸音清,心界向左扩大,心率85次/分,胸骨左缘第2~3肋间闻及4/6级连续性吹风样杂音。心超:右房室增大,右室增厚约10mm,肺动脉瓣环内径22mm,肺动脉瓣环处见隔膜样回声,瓣膜启闭欠清,连续多普勒估测跨瓣压差约为53mmHg,肺动脉瓣中重度返流,左心室不大,左室射血分数(LVEF) 74%,室间隔未见残余分流。 肝肾功能、电解质、凝血功能、血常规正常。 心电图:完全性右束支传导阻滞,QRS波宽度 162ms。
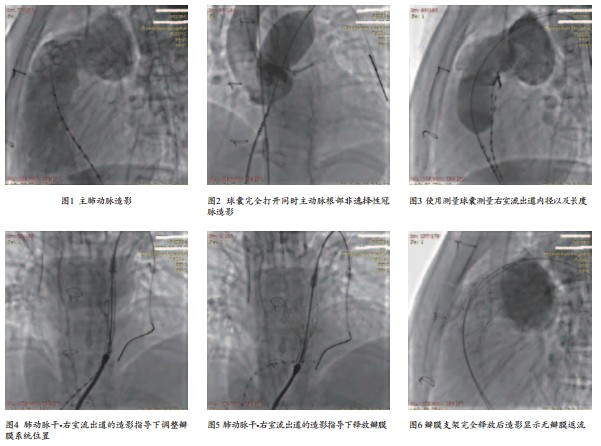
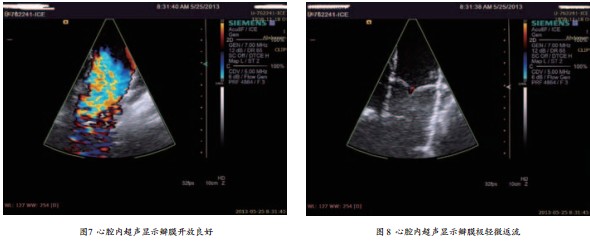
患者于心导管室静脉复合麻醉下行经皮肺动脉瓣置入术(PPVI)。常规消毒铺巾,分别穿刺左侧股动静脉并置入6F动脉鞘。穿刺右侧股静脉,预先放置PROGLIDE血管缝合装置,置入8F血管鞘。从右侧股静脉送入6 F MPA导管,行右心导管检查。将5F 黄金表猪尾巴导管从股静脉送至肺动脉干处进行造影观察肺动脉瓣返流情况(图1),并在头位45度加左前斜20度、侧位观察右室流出道、肺动脉干及其分支的走形并测量右室流出道、肺动脉干内径、肺动脉瓣环内径。将TSCMG-35-260-LESDC 超硬导丝导入左肺动脉远端,在该导丝指引下送入7 F 34 mm X 70 mm Amplatzer测量球囊导管送到右室流出道-肺动脉干处。从左侧股动脉处送入6F猪尾巴导管至主动脉根部,将测量球囊完全打开同时行主动脉根部非选择性冠脉造影,观察冠状动脉与肺动脉解剖毗邻关系及其是否受到球囊压迫(图2),结果显示左冠显示清楚,未见到压迫。观察体位为侧位及左前斜25加头位45度。从右侧股静脉送入6F 猪尾巴导管至肺动脉干处,适度打开测量球囊并行肺动脉造影,使得测量球囊刚好堵住右室流出道(球囊能随心跳上下滑动、造影不会出现返流),测量此时测量球囊的腰部狭窄处的内径以及长度(图3),以作为瓣膜型号选择的依据。退出右侧股静脉的8F血管鞘,沿超硬导丝送入21F输送鞘。选择VENUS-P瓣膜,于冰盐水中通过装配系统将瓣膜装配于19 F输送系统(输送鞘)。DSA取头位45度,在超硬导丝引导下将装有瓣膜的输送系统送至肺动脉-右室流出道处。将猪尾巴导管送至肺动脉干处行血管造影,以显示瓣膜在肺动脉干-右室流出道的位置(包括头位45度和侧位),调整瓣膜的位置,使得瓣膜处于合适位置(图4)。DSA机取头位45度,开始释放瓣膜,过程中不断行肺动脉干造影并调整瓣膜的位置,在瓣膜支架打开前回撤猪尾巴导管至右心室并右心室行造影指导瓣膜的释放(图5)。瓣膜位置理想后,完全释放瓣膜(图6)。退出瓣膜系统,经加硬导丝送入多通道导管,复查肺动脉干造影及心腔内超声观察肺动脉瓣返流情况(图7~8),测量肺动脉干压力、右心室压力。拔除鞘管,使用预放的动脉穿刺闭合装置缝合21F鞘管静脉穿刺点、余穿刺点压迫止血,等待麻醉苏醒。抗生素静脉治疗3天。术中静脉给予普通肝素3000u,造影剂500ml。术后送入监护室,以阿司匹林 0.1gqd(1月)。
经皮肺动脉瓣置入术(PPVI)是最早运用于临床的经皮瓣膜置换技术,2000年即有临床成功运用的报道。目前国外PPVI 完成4000例左右,国内之前还未有临床应用的报道,本例为国内首例人体PPVI 术。
在国内,法洛四联症(TOF)等有右室流出道(RVOT)及肺动脉狭窄的患者行手术矫正的过程中普遍行RVOT跨瓣补片术(RVOT、肺动脉纵向切开后加补片以扩大管腔内径),以解除RVOT及肺动脉狭窄,使得肺动脉瓣环扩大,瓣叶对合不良(有些患者术中甚至切除病变的肺动脉瓣),导致明显的PR;而国外许多中心则会在RVOT置入带瓣膜人工血管,虽然短期之内不会有PR,但长期应用后,人工血管会出现钙化导致RVOT梗阻,且其生物瓣膜会出现功能退化导致瓣膜关闭不全或狭窄,这种综合征被称之为RVOT功能不全。慢性PR可导致右心负荷增加、右心扩大,继而引起右心衰、心律失常(室早、室速、室颤、房扑、房颤)甚至是猝死,同时由于扩大的右心挤压左心室导致左心功能不全(左室射血分数下降、运动耐力降低),进一步恶化患者的临床状态。由于长期的PR会对患者长期预后造成不良影响,人们就提出肺动脉瓣置换(PVR)的治疗方法,包括外科PVR及PPVI 术。PPVI 相对于外科PVR创伤性更小、手术风险更低,对于外科手术高危患者尤为合适。
来源: 医心评论第65期



 京公网安备 11010102002968号
京公网安备 11010102002968号