PCI 术后接受非心脏外科手 术者围术期抗栓治疗策略
发布于:2013-07-16 17:51
文 / 马礼坤 张晓红 安徽省立医院
马礼坤 安徽省立医院;心内科副主任,安徽省首批学术与技术带头人;教授、主任医师、硕士研究生导师,中国医疗保健促进会心血管专业委员会委员,中国医药生物技术协会心电学技术分会委员,安徽省病理生理学会危重病分会副主任委员,安徽省心血管学会委员,被国家卫生部聘任为冠心病介入诊疗的培训导师。
编者按:随着经皮冠状动脉介入治疗(PCI)的深入开展,其已经成为治疗冠心病的重要手段之一,然而有资料研究表明,接受冠脉支架置入术后仍需要接受外科手术的患者并不少见,所以围术期就会面临如何使用抗血小板药物的问题。在2013年CIT 大会上,马礼坤教授就这一相关题目分享了他的观点:即PCI 术后需要接受外科手术者,围术期主要心血管事件(MACEs)的发生与支架置入时间的长短有关,其发生机制有很多方面;而影响PCI 术后非心脏外科手术(NCS)预后的主要因素为PCI 术至外科手术的间隔时间和停用双联抗血小板治疗。由于在NCS 围术期会存在ST 和出血的风险,所以对PCI 术后择期NCS 的时间选择和非择期NCS 围术期抗血小板治疗要引起重视,下文马礼坤教授将和我们详细分享、探讨以上观点。
经皮冠状动脉介入治疗(PCI)是冠心病的重要治疗手段之一。据统计全球每年有超过100 万以上的患者接受PC术,其中大约85% 的患者至少置入1 枚以上的支架。研究表明,PCI 术后过早停用双联抗血小板治疗的患者支架内血栓(ST)形成的风险明显增加,并可导致心肌梗死、死亡等严重心血管事件的发生。目前国内外现行指南均推荐置入药物洗脱支架(drug-eluting stent, DES)后双联抗血小板(阿司匹林和ADP 受体拮抗剂)治疗至少1 年,置入金属裸支架(BMS)后双联抗血小板治疗至少1 个月以上,以降低晚期ST 形成的风险。然而研究资料表明,接受冠脉支架置入术后1 年内约有4%~10% 的患者由于各种原因需要接受外科手术或相关的侵入性操作,在支架术后1 年以上的患者中需要施行类似外科手术的比例更高。对于这些PC术后需要接受外科手术的患者,围手术期将面临继续服用抗血小板会使手术相关的出血风险增加,而停用抗血小板药可能会导致ST 的发生这样两难的境地,因此依据具体临床情况权衡利弊,制定合理的抗栓治疗方案显得尤为重要。本文就PCI 术后需要接受非心脏外科手术(NCS)者围术期抗栓治疗策略做一综述。
1. PCI 术后外科围术期主要心血管事件的发生率增高
1.1 PCI 术后外科围术期主要心血管事件的发生率
PCI 术后需要接受外科手术者围术期发生心脏性死亡、心肌梗死等主要心血管病事件(MACEs)的风险明显增高。Vincenzi 等对支架术后1 年内进行非心脏外科手术的103 例患者进行研究显示,44.7% 的患者术后发生了各种心血管病相关的并发症,且多数是出现在支架术后早期外科手术者。其中死亡4.9%,死亡患者中除2 例因为出血死亡外,其余均证实属于心源性死亡。支架置入术后近期外科手术(35d 内)者发生心脏事件的风险是远期手术(90d 后)者的2.11 倍。Riddell 等总结了八项回顾性临床研究,结果显示PCI 术后非心脏手术围术期死亡率为2.5%~21.4%。且置入BMS 者外科围术期MACEs 发生率随着外科手术距离PCI术后时间的延长而降低,尤其是支架置入90d 以后出现较为明显的下降;而对于置入DES 的患者即使是在支架置入1 年后接受外科手术者围术期MACEs 的发生也仅呈中度的下降趋势。
1.2. 影响PCI 术后NCS 围术期MACEs 的主要临床因素
影响PCI 术后NCS 围术期预后的主要临床因素为PCI术至外科手术的间隔时间和停用双联抗血小板治疗。许多研究表明,PCI 术后过早地进行NCS 者 MACEs(包括支架内血栓、死亡和心肌梗死等)的发生率较高。Savonitto 等统计分析了来自Mayo、Cleveland、Rotterdam 和Scottish 等中心的研究数据,结果显示无论是置入DES 支架还是BMS支架,PCI 术后1 月内NCS 围手术期MACEs 发生率甚至高达30%,PCI 术后2~6 个月和6 个月以后MACEs 的发生率分别为10%~15% 和<10% 。Alshawabkeh 等对四项有关DES 术后NCS 患者预后的临床研究进行荟萃分析,结果显示DES 术后6 个月内、6~12 个月、>12 月NCS 围术期ST发生率为2.33%、1.71% 和0.86%,其中65.4%ST 病例停用了双联抗血小板治疗。RECO 研究是一项纳入1134 例冠状动脉支架患者,接受择期或紧急NCS 或其他侵入性操作的的前瞻性、多中心、观察性队列研究,结果显示与外科手术后MACEs 发生有关的术前独立相关因素分别为术前停用双联抗血小板治疗超过5 天、血红蛋白<10 g/dl、肌酐清除率<30 ml/min 及急诊或高危外科手术。RECO 研究结果同时显示围术期停用双联抗血小板治疗时间越长,MACEs的发生率越高。
1.3 影响PCI 术后NCS 围术期MACEs 发生的机制
其机制可能是多方面的,包括:
(1)围术期应激反应、疼痛和血流动力学的不稳定会导致冠脉血供减少,心肌耗氧量增加,易发生心肌缺血、缺氧;
(2)在NCS 术后早期应激反应激活交感神经系统,导致神经内分泌激素如肾上腺素、去甲肾上腺素、皮质醇、肾素等释放;
(3)手术创伤导致高凝状态,失血、血液稀释和低温等都可以导致心脏不良事件的发生,同时交感神经兴奋对血管壁斑块的剪切力增加,又可导致冠脉斑块的破裂,诱发急性心肌梗死。由于90% 左右的PCI 术会置入支架,绝大多数研究认为外科手术对凝血的影响、围术期促凝因子增加、纤溶降低等因素导致的术后高凝状态,由此造成的ST 形成是外科围术期心脏不良事件增加的重要因素。此外,由于PCI 术中球囊扩张造成的血管损伤,局部炎症反应表达增强,内皮损伤加重,促凝因子局部进一步激活;而且支架本身也会导致炎症反应和促凝改变;在PCI 术后尤其是DES 支架近期内支架内皮化不全,而为了减少术中出血往往需要中断双联抗血小板治疗,显然会增加围术期ST 的发生率。围术期一旦发生ST 其结果往往是灾难性的,常伴有较高的急性心肌梗死发生率和死亡率。
2. PCI 术后NCS 围术期ST 形成和出血风险评估
2.1 NCS 围术期ST 形成的风险
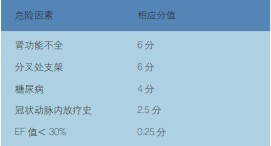
评估ST 形成的风险包括患者的临床因素:如高龄、糖尿病、肾功能不全、肥胖、左室功能不全、急性冠脉综合征、冠脉多支病变、过早停用抗血小板药物、抗血小板药物抵抗等;另一方面是与PCI 相关的因素包括长支架、多枚支架置入或重叠、左主干或前降支近端支架、开口或分叉病变、小血管支架置入、支架扩张不全或贴壁不良、术中曾发生无复流和慢复流、支架内再狭窄、冠脉内放射治疗,以及支架术后支架内皮化不完全和与手术相关的机体高凝状态等。有研究提出了支架术后发生ST 常见的危险因素评分见(表1),其中0~6 分为低危,7~9 分为中危,10~13分为高危,14~19 分为极高危。
表1 晚期ST的危险因素评分表
2.2 NCS 围术期出血的风险
PCI 术后持续应用双联抗血小板治疗NCS 出血的风险肯定会增加。研究显示,PCI 术后施行NCS 时继续氯吡格雷与阿司匹林合用,可以使围术期出血的相对危险度增加约25%~40%,再次手术止血的比例也明显增高;且阿司匹林和氯吡格雷双联抗血小板治疗较单用阿司匹林者出血风险增加0.4%~1.0%。尽管也有研究认为,围术期继续双联抗血小板治疗并不增加严重出血的风险,也不增加外科手术的死亡率和致残率,但PCI 术后患者在施行NCS 前仍然必须充分评估和考虑术中出血的风险、出血后果及是否伴有其他出血因素。按照外科手术本身出血可能性的大小和出血后造成临床后果的严重程度可将NCS 分为高危、中危和低危出血风险手术。低危出血风险的手术指牙科操作皮肤及白内障手术等;高危出血风险的手术包括主动脉或其他大血管手术(包括周围血管手术)、神经外科手术、前列腺活检或手术、视网膜手术、脊柱手术等出血后临床后果相对严重;其余手术多属中危出血风险。对于那些高危出血风险的手术如神经外科手术或有严重出血病史的患者来说,持续抗血小板治疗应该警惕出血危险的增加带来严重后果。美国胸科医师学会(ACCP)建议下列手术前应停用阿司匹林和氯吡格雷:①主动脉瘤手术;②肾活检;③颅内手术或脊柱手术;④前列腺或膀胱手术;⑤大的肿瘤手术;⑥大的骨科手术等。其他种类的择期NCS 手术均可在服用阿司匹林或氯吡格雷的情况下进行。
3.PCI 术后NCS 围术期抗栓治疗策略
3.1 择期NCS 的时间选择
一般来说,PCI 术后不主张过早进行外科手术。除非急诊,所有择期NCS 都主张延期到PCI 术后一定的间隔时间再施行。有关择期NCS 的合理间隔时间,2007 年ACC/AH指南建议对于单纯球囊扩张者宜为PCI 术后2~4 周后;置入BMS 者延迟至少4~6 周,最好能在3 个月以后再进行以确保支架后血管内皮修复和支架表面内皮化的完成;而对于置入DES 者因内皮愈合延迟,过早停用双联抗血小板药物会明显增加支架内晚期血栓的发生率,一般建议尽可能在支架术后12 个月以上再进行择期NCS。属于择期非急诊外科手术者经过上述相应的间隔时间后实施外科手术时停用双联抗血小板治疗发生血栓的风险明显减少,可以依据临床情况围术期停用一种或两种抗血小板药,待外科术后出血停止再恢复相应的抗血小板治疗。
3.2 非择期NCS 围术期抗血小板治疗策略
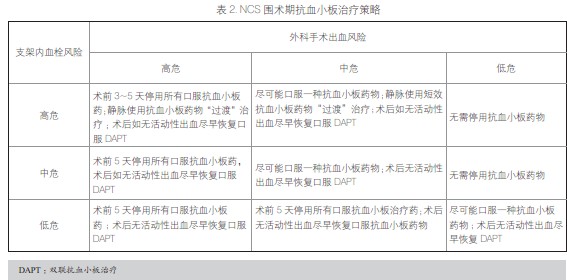
对于PCI 术后需要接受非择期或者急诊外科手术者制定合理的抗栓治疗方案显得尤为重要,目前对这类患者围术期的处理意见尚不统一,术前应该由心内科、外科以及麻醉科进行充分的评估, 制定围术期最佳的个体化抗栓治疗方案。首先要考虑的是支架术后至外科手术的间隔时间,ACC/AHA 指南均推荐若BMS 置入后4~6 周内或DES 术后1 年内需行紧急手术,建议术前停用氯吡格雷,但尽可能续用阿司匹林,并在术后尽快恢复服用氯吡格雷。此外,支架的类型(BMS 还是DES)、术后出血风险、手术医生的经验和患者的临床特征等在制定抗栓策略时都是需要认真考虑的问题。围术期是否停用抗血小板药物取决于患者外科手术出血和支架内血栓形成的风险是否属于高危、中危和低危而采取相应的处理策略(见表2)。
对于血栓高危的患者,包括因急性冠脉综合征置入药物洗脱支架、有支架内血栓史、左主干或分叉支架等,非择期外科手术围术期可以短期静脉使用GP IIb / IIIa 受体拮抗剂进行过渡治疗,过渡治疗中推荐使用半衰期相对较短的替罗非班或依替巴肽,具体方法为:如果不是神经科或眼科手术,对于围术期可续用阿司匹林的PCI 患者,应在术前5 天停用氯吡格雷,并在停用1-2 天后开始静脉滴注GP IIb / IIIa 受体拮抗剂,至术前4-6h 停用;术后4h 重新再予静脉滴注,直至术后24 小时恢复口服氯吡格雷为止,恢复服用氯吡格雷的负荷剂量仍为300mg,并继以常规剂量(75mg/d)口服。小样本研究结果显示应用GP IIb / IIIa 抑制剂的过渡疗法并未增加围术期的出血风险,同时也能有效防范支架内血栓等MACEs 的发生。目前也有围术期采用普通肝素或低分子肝素替代抗血小板治疗的方法,但抗凝并不能代替阿司匹林等的抗血小板作用,目前采用GPIIb/IIIa 受体拮抗剂作为过渡治疗较肝素或低分子肝素更为普遍。必须指出的是目前有关“过渡”治疗的临床疗效尚缺乏足够的循证医学证据,但在采取现有的“过渡”治疗策略期间发生围术期支架内血栓者也仅见于个案报道。
ESC 指南推荐一旦手术后止血良好,可在术后24 小时恢复阿司匹林或氯吡格雷的应用。法国麻醉和重症医学协会(SFAR)推荐如果术后恢复应用阿司匹林,首剂负荷量应>160mg ;如术后恢复氯吡格雷,首剂应给予300mg 的负荷量,以利于短时间内达到最大抑制血小板功能的作用,从而防止和减少围术期支架内血栓的发生率。
4. 小结
PCI 术后1 年内因各种原因需要接受NCS 者并不太少见,如何减少因使用抗血小板药引起的外科围术期出血风险增加和避免停用抗血小板药导致的支架内血栓形成往往是一个比较棘手的问题,为此临床上必须根据每个患者的具体情况制定个体化的处理策略。一般主张置入支架尤其是药物洗脱支架后的择期NCS 尽量推迟到预计支架已充分内皮化后的一定间隔时间进行,置入BMS 者最佳时间应是PCI 术后至少90 天, 置入DES 应在12 个月以上。如果属于急诊外科手术,则需要充分考虑外科手术出血风险的高低和出血后临床后果的严重程度,并结合停用双联抗血小板药后可能发生支架内血栓的危险度高低采取不同的抗栓治疗方案,属于出血风险较低的外科手术可以在不停用双联抗血小板治疗的同时进行;相反对于支架内血栓形成风险很低者可以暂时停用一种甚至同时停用两种抗血小板药,待术后出血停止再重新使用;但对于ST 高风险的患者外科围术期需要采用肝素或GPIIb/IIIa 抑制剂的过渡治疗策略,并尽量缩短停用双联抗血小板治疗的时间。NCS 围手术期合理选择特殊抗栓策略、恰当把握抗栓强度、正确处理抗血小板与出血之间的矛盾,对降低外科围手术期MACEs 风险至关重要。
来源: 医心评论



 京公网安备 11010102002968号
京公网安备 11010102002968号